SUVmax 7.4!16岁少女腹腔“肿瘤大爆发”?宾夕法尼亚大学庄红明团队揪出幕后“伪装者”!
- 2026-04-16 04:36:20



16岁,本该是无忧无虑的年纪。
但对于这位女孩来说,生活却是一场与死神的拉锯战。她被确诊为转移性黑色素瘤,且伴有肺转移 。
为了活下去,她接受了目前最前沿的“组合拳”治疗:PD-1抑制剂(纳武单抗) + BRAF/MEK抑制剂 。
治疗一年后,病情似乎稳住了。但就在最近,她突然开始剧烈腹痛、呕吐,持续了整整9天 。
噩耗似乎接踵而至。
增强CT一扫,医生倒吸一口凉气:肠系膜上出现了“靶环状”强化病灶,周围全是浑浊的脂肪条索(图1)。
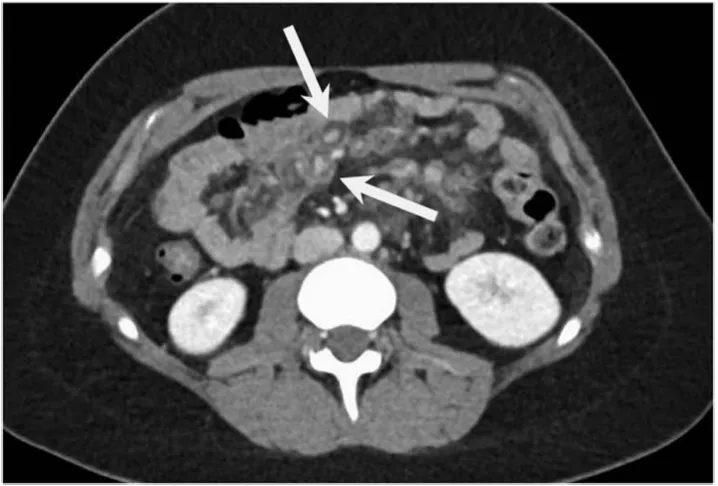
图1.腹部CT显示环靶征及脂肪条索影
放射科医生的第一反应是:坏了,肿瘤复发了,腹腔转移!
如果是复发,意味着现在的治疗方案全部失效,女孩的生命可能进入倒计时。

为了进一步确诊(或者说为了确认“死刑”),医生安排了 FDG PET/CT。
图像出来的瞬间,所有人的心都沉到了谷底。
上腹部那一团浓聚的黑影,触目惊心(图2A)。肠系膜上的结节摄取极其活跃,SUVmax 高达7.4(图2B)!
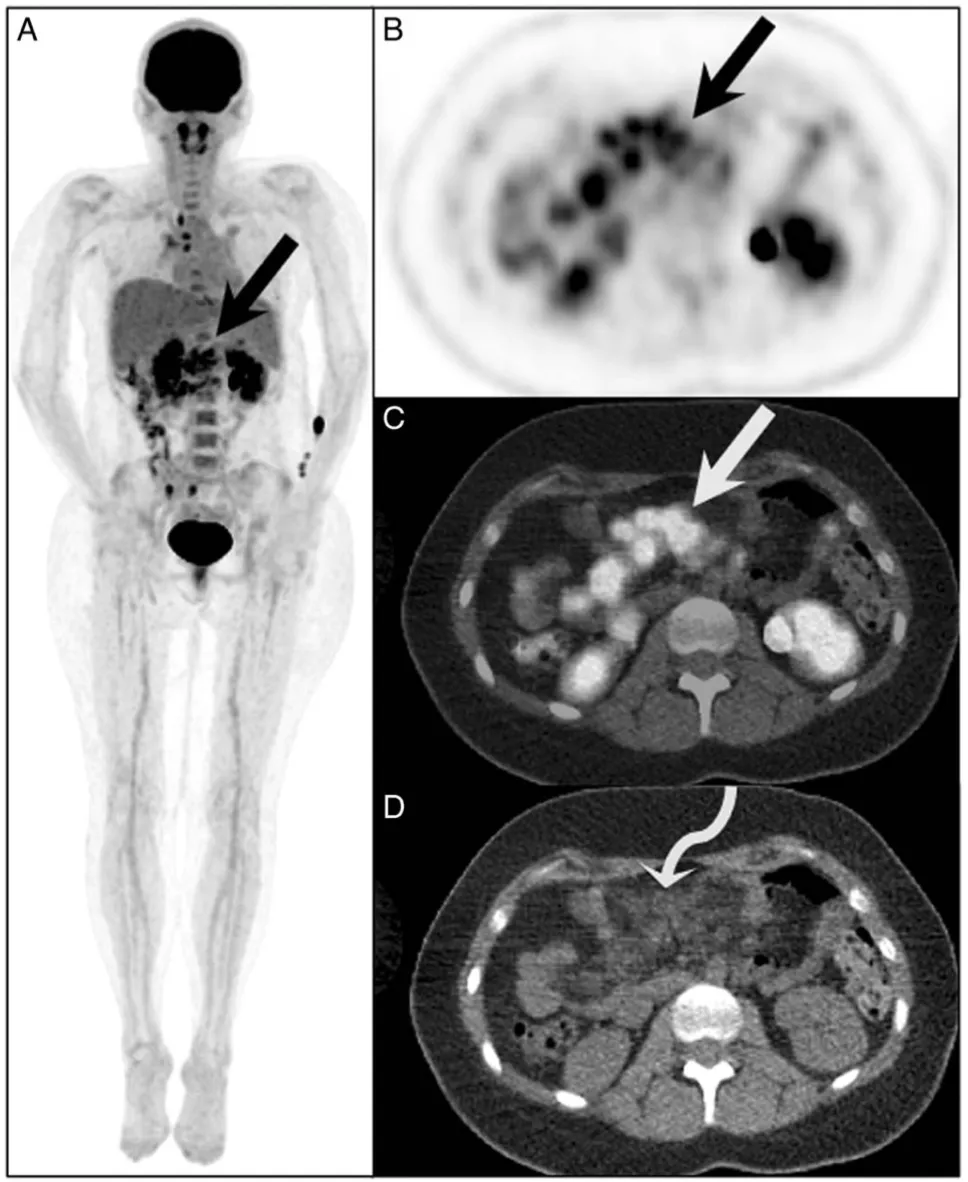
图2.患者PET/CT图像显示肠系膜区多发高代谢灶
CT显示强化,PET显示高代谢(SUV 7.4),在传统的影像诊断逻辑里,这几乎就是“肿瘤多发转移”的铁证。
那么,这个女孩将被迫停用纳武单抗,转向副作用更大、效果未知的二线治疗。
但是,真相真的如此吗?

核医学科的医生没有急着下结论。他们复盘了整个病例,发现了一个疑点:
为什么只有肠系膜?为什么其他部位(如之前的肺转移)没有动静?
他们决定引入第三只眼——MRI。
同一天做的MRI T2加权像显示,这些“肿瘤结节”周围有着广泛的弥漫性水肿信号(图3)。
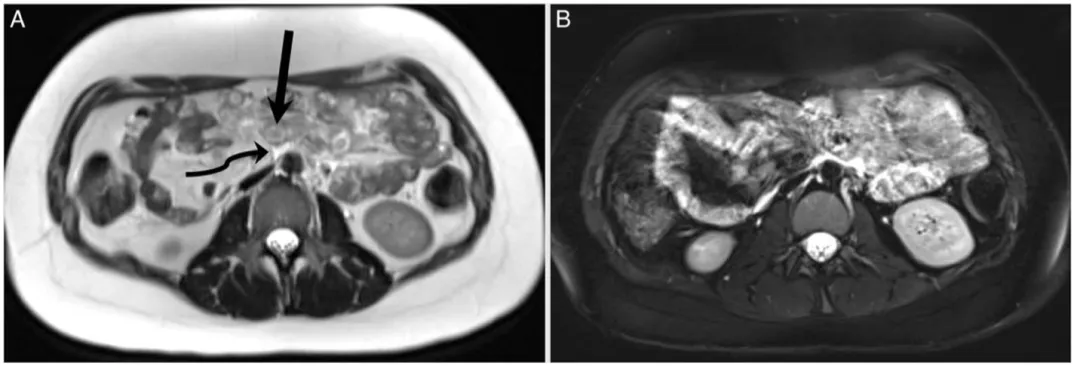
图3.患者MRI图像显示肠壁弥漫性水肿
紧接着,实验室检查传回消息:患者的 C反应蛋白(CRP)和细胞因子水平显著升高 。
拼图终于完整了:
高代谢(FDG avid):代表活跃的糖酵解,可以是肿瘤,也可以是炎症。
T2高信号水肿:更倾向于炎性渗出。
用药史:PD-1抑制剂(纳武单抗)会激活免疫系统,不仅攻击肿瘤,也会攻击正常组织。
神反转诊断:免疫相关不良反应(irAE)——肠系膜脂膜炎(Mesenteric Panniculitis, MP)!
这团SUV 7.4的“黑火”,不是肿瘤的疯狂反扑,而是免疫系统“杀红了眼”误伤了肠系膜脂肪。

因为这个精准的判断,医生并没有停掉女孩救命的PD-1抑制剂。
她仅仅接受了他莫昔芬(Tamoxifen) 对症治疗(用于预防肠系膜纤维化)。
奇迹发生了。
随访的 PET/CT 显示,腹腔的高代谢病灶完全消失(图像未显示)。女孩的症状缓解,继续接受着有效的抗肿瘤治疗。
试想,如果当初一看到SUV 7.4就判了“死刑”,后果不堪设想。

随着免疫治疗(ICI)的普及,我们在阅片室会遇到越来越多的“假性进展”。基于宾夕法尼亚大学庄红明教授团队这篇发表在
2026年 Clinical Nuclear Medicine上的最新个案 ,我们总结了以下避坑 SOP:
问病史(History taking):看到PET/CT上有奇怪的“新发病灶”,先问一句:“病人在用PD-1/PD-L1吗?”如果有,脑子里要永远绷着一根弦:免疫相关不良反应(irAEs)。
识图像(Pattern Recognition):肠系膜脂膜炎(MP)的典型特征,CT:脂肪条索影(Fat stranding),可能出现“靶征” ;PET:甚至可以很高代谢(本例SUVmax 7.4),不要被数值吓倒。MRI:T2像上的水肿是鉴别利器。
看指标(Lab Correlation):结合CRP、红细胞沉降率(ESR)等炎症指标。如果指标飙升且与影像吻合,优先考虑炎症。
核医学的价值,不仅仅是发现肿瘤,更是保护患者免受误诊的伤害。
在免疫治疗时代,我们要练就一双分辨“真假美猴王”的火眼金睛。
您在临床上遇到过PD-1治疗后的“假性进展”吗?最高的SUV值到过多少?欢迎在评论区分享您的惊险时刻!
参考文献
https://journals.lww.com/nuclearmed/abstract/2026/01000/mesenteric_panniculitis_mimicking_metastases_from.14.aspx
阅读量即将破10W+!
核医学精彩文章推荐
LVA共识被核医学专家理性怒怼15天后,国家卫健委正式叫停!
已宣判!医生发现肿标升高未预警,PET/CT确诊肿瘤后家属起诉医院
浙江省PET检查收费形式巨变,受益方到底是谁
我们的权益:放射假和放射津贴 — 你get到了吗?
三明医改下的核医学科竟然成为公立医院最香科室,遥遥领先!
最贵有多贵?盘点2024年PET设备中标价格
强强联合!于金明院士携手程震教授在核医学顶刊发表最新研究成果
惊喜!西南医科大学核医学科病例登顶放射学顶刊Radiology
为什么说做即将纳入医保的 PET/CT 是 “磨刀不误砍柴工” ?
 ↓↓ 欢迎进入鼎湖学堂
↓↓ 欢迎进入鼎湖学堂

